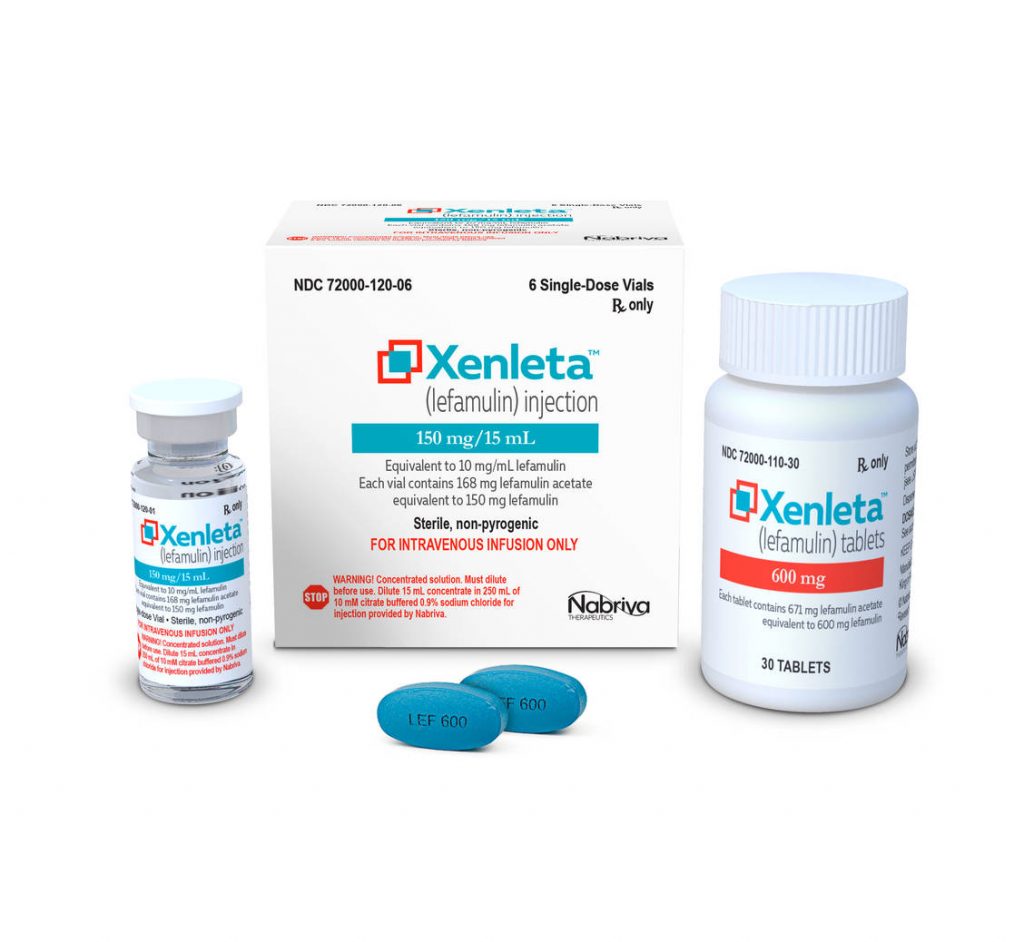
Die FDA (Food and Drug Administration) hat am 19. August 2019 mit Lefamulin(Xenleta) ein neues Antibiotikum in den USA zugelassen. [1] Es ist der erste systemisch verfügbare Pleuromutilin-Antibiotikum zur Behandlung von Erwachsenen (Community-Acquired Bacterial Pneumonia, CABP) mit ambulant erworbener bakterieller Pneumonie überhaupt. Damit gilt es als neuartiges Antibiotikum mit einem neuartigen Wirkmechanismus. Daher soll es auch immer dann eingesetzt werden herkömmliche Antibiotika wegen Resistenzen nicht mehr wirken.
Lefamulin (Xenleta) neues Antibiotikum: von Nabriva Therapeutics
Das von Nabriva Therapeutics entwickelte Antibiotikum Lefamulin (Xenleta) schafft es 2014 in das FDA Expedites Program. Dieses Programm beschleunigt die Zulassung. Im falle von Lefamulin (Xenleta) bekam es den Status Fast Track. Diesen Status erhalten neue Medikamente, wenn diese als Einzelmedikament oder als Kombination mit anderen Medikamenten das Potential haben lebensbedrohliche Krankheiten zu behandeln. Allein Theoretische Überlegungen oder Erklärungen könnten ausreichen. Die FDA hat dann 60 Tage Zeit um diese zu entscheiden. Nach der Zulassung schoss der Aktienkurs des irischen Biopharmazeutischen Unternehmens in die Höhe, später viel der Kurs wieder auf die Baseline vor der Zulassung.
Der Wirkmechanismus von Lefamulin (Xenleta)
Lefamulin (Xenleta) gehört zur Gruppe von Pleuromutiline- Antibiotika. Pleuromutiline sind Naturstoffe, die in der Regel aus Pilzen stammen. Lefamulin hemmt die PBS (Proteinsynthese). Das Peptidyltransferase-Zentrum der 50S-Untereinheit der Ribosomen wird von Lefamulin gebunden. Das neuartige Antibiotikum soll aufgrund ihrer Struktur zudem zu geringerer Resistenzbildung neigen. Lefamulin wird es ab September in den USA einmal als orale (600mg) und einmal als intravenöse (150mg) Darreichungsform geben. Die Therapiedauer beträgt ca. 7 Tage. Die Therapiekosten liegen bei 275 Dollar bei der oralen formulieren und 205 Dollar bei der Intravenösen. Der Antrag für die Zulassung von Lefamulin(Xenleta) bei der Europäischen Arzneimittelagentur ist eingegangen.
Nebenwirkungen
Die beiden Phase-III-Studien LEAP 1 und LEAP 2 mit insgesamt knapp 1300 CABP-Patienten waren zufriedenstellen. [2] Hier wurden als Vergleiche Moxifloxazin und Linezolid verglichen. Nebenwirkungen wie Durchfall, Erbrechen und erhöhte Leberenzymwerte waren gehörten zu häufigsten.
Quellen
- FDA approves new antibiotic to treat community-acquired bacterial pneumonia Link zugegriffen am 22. August 2019
- Clin Infect Dis. 2019 Feb 4. doi: 10.1093/cid/ciz090. Efficacy and Safety of IV-to-Oral Lefamulin, a Pleuromutilin Antibiotic, for Treatment of Community-Acquired Bacterial Pneumonia: The Phase 3 LEAP 1 Trial. File TM Jr1, Goldberg L2, Das A3, Sweeney C2, Saviski J2, Gelone SP2, Seltzer E4, Paukner S5, Wicha WW5, Talbot GH6, Gasink LB2. Link zugegriffen am 22. August 2019
 Blog über Arzneimittel & Gesundheit Neues aus der Pharmawelt. Nachrichtne über neue Arzneimittel, Pharmazie und Gesundheit
Blog über Arzneimittel & Gesundheit Neues aus der Pharmawelt. Nachrichtne über neue Arzneimittel, Pharmazie und Gesundheit