Ein neues, vielversprechendes Arzneimittel gegen Schizophrenie steht wohlmöglich in den USA kurz vor der Zulassung. Der Wirkstoff Lumateperon wird vom US-Biotech Unternehmen Intra Cellular Therapies entwickelt. Die Lizenz für den neuen Wirkstoff hat Bristol-Myers Squibb. Der Zulassungsantrag wurde Ende 2018 bei der FDA (Food and Drug Administration) eingereicht. Das PDUFA-Zieldatum wurde aber vor Kurzem nochmald um drei Monate auf den 27. Dezember 2019 verlängert.
„PDUFA-Termine sind Fristen bzw. Deadlines bis zu denen die FDA neue Arzneimittelanträge prüfen muss. Normalerweise hat die FDA dazu 10 Monate Zeit. Bei seltenen, schweren Krankheiten oder bahnbrechenden, neuen Arzneimitteln nur 6 Monate. Im Gegenzug darf die FDA eine Gebühr erheben (User fee). Meistens kommt es jedoch zu Verlängerungen, da die FDA mehr Zeit benötigt den Überprüfungsprozess abzuschließen.“ Verlängerungen werden meist negativ gewertet.
Lumateperon bei Schizophrenie: weitere Indikationen werden evaluiert
Seitens Intra Cellular Therapies soll zudem eine Erweiterung der Indikaton erforscht werden. Folgende neue Indikationsgebiet werden noch evaluiert: Depressionen wie Bipolare Störungen und spezielle Formen bei Demenz (Phase III) sowie Schlafstörungen (Phase II).
Schizophrenie ist eine schwere Krankheit
Die Schizophrenie ist eine psychische Erkrankung mit Psychosen. Die Wahrnehmung, Denken und Motorik werden je nach Schweregrad stark beeinträchtig. Oft hören die Betroffenen nicht vorhandene Stimmen oder haben Verfolgungswahn sowie Halluzinationen. Die Folgen sind sozialer Rückzug, Antriebslosigkeit und Freudlosigkeit. Schizophrenie ist eine schwere Krankheit. Sie tritt oft in jungen Jahren (16 – 30) auf. Meist muss beispielsweise die Ausbildung oder das Studium für eine gewisse Zeit aussetzt werden. Man schätzt, dass rund 0,5 bis 1 % der Bevölkerung an Schizophrenie erkrankt. Laut einer Studie aus dem Jahre 2013 hatten weltweit 23.6 Millionen Menschen Schizophrenie. [1] Es gibt verschiedene Formen und Klassen von Schizophrenien und können schubweise oder auch chronisch verlaufen. Ein Schub kann mehrere Wochen oder Monate dauern. Danach haben die Betroffenen ein paar Monate Ruhe bis zu einem neuen Schub. Bis heute ist die Krankheit nicht heilbar und die Lebenserwartung sinkt. Neue Medikamente ermöglichen aber ein nahezu beschwerdefreies Leben.
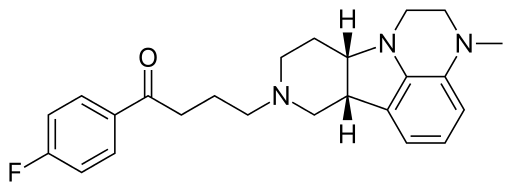
Der Wirkmechanismus von Lumateperon bei Schizophrenie

Der neue Wirkstoff Lumateperon von Intra Cellular Therapies birgt neue Hoffnungen für Schizophrenie-Patienten. Lumateperon ist ein Atypisches Neuroleptikum. Als 5-HT2A-Rezeptorantagonist und Dopamin- und Serotonin-Transporter Modulator soll es ein völlig neues Wirkmechanismus haben. [2] [3] Laut Ergenissen der Klinischen Phase II sollen eine tägliche Einnahme von 60 mg eine Verbesserung der Psychose bewirken. [4] Darüber hinaus soll Lumateperon in Vergleich zu Risperidon (Goldstandart) Nebenwirkungsärmer sein. Beispielsweise keine Gewichtszunahme und keine QTC-Verälngerung. Ein weiterer positiver Nebeneffekt bei Lumateperon: es soll auch bei Begleiterscheinungen der Schizophrenie, beispielsweise Depressionen und bei sozialem Rückzug helfen. Risperidon konnte diese positiven Effekte nicht zeigen [2] [5]. Lumateperon soll auch aufgrund seiner positiven Effekte bei den Stoffwechselparameter, im Gegensatz zu anderen Neuroleptika, das Risiko für Diabetes oder Herz-Kreislauf Erkrankungen nicht erhöhen. Daher soll das neue Mittel eine signifikante Verbesserung im Hinblick auf die langfristige Sicherheit und Verträglichkeit sein. [2] Erst bei der doppelten Tagesdosis, also 120mg war bei 32,5% der Probanden die häufigste Nebenwirkung: Sedierung, bzw. Schläfrigkeit. Eine Zunahme von Selbstmordgedanken oder extrapyramidale Symptome konnte nicht beobachtet werden. [5]
Lumateperon bei Schizophrenie: Worst-Case-Szenario
Es könnte aber auch ein Worst-Case-Szenario mit vollständiger Ablehnung der Zulassung des Lumateperon bei Schitzophrenie seitens der FDA eintreten. Nur ein Erfolg von zwei Phase III-Monotherpie-Studien schwächt die Zulassungschancen. Die Studie mit der Kennung 401 welche nur in der USA durchgeführt wurde konnte keine zufriedenstellenden Ergebnisse liefern. Die Studie mit der Kennung 404, welche mit zwei Drittel in Russland oder Kolumbien durchgeführt wurde erreichte ihre primären und sekundären Endpunkte. Bis zum 27. Dezember 2019 soll nun endgültig über die Zulassung entschieden werden. Für Intra-Celluar Therapies wäre eine Ablehnung eine Katastrophe, da die Kraft jahrelang in Lumateperon konzentriert wurde. Eine Zulassung hingegen – im Idealfall mit den zusätzlichen Indikationen – wäre für das Unternehmen ein Sechser im Lotto. Denn der Markt bei diesen Indikationen ist weltweit sehr groß. Weitere Nachrichten bis 27. Dezember werden richtungsweisend sein.
Intra-Cellular Therapies ist ein US-Biotech Unternehmen mit Sitz in New York. Hauptfokus der Forschung ist die Behandlungen bei Störungen des zentralen Nervensystems. Hauptprodukt der Pipeline ist das Lumateperon.
Quellen
- Intra-Cellular Therapies Announces Further Analyses of the Phase 2 Clinical Trial of ITI-007 in Schizophrenia at the 168th Annual Meeting of the American Psychiatric Association. Link zugegriffen am 07. August 2019
- Gretchen L. Snyder,corresponding author Kimberly E. Vanover, Hongwen Zhu, Diane B. Miller, James P. O’Callaghan, John Tomesch, Peng Li, Qiang Zhang, Vaishnav Krishnan, Joseph P. Hendrick, Eric J. Nestler, Robert E. Davis, Lawrence P. Wennogle, and Sharon Mates. Functional profile of a novel modulator of serotonin, dopamine, and glutamate neurotransmission. Psychopharmacology (Berl). 2015; 232: 605–621. Published online 2014 Aug 15. doi: 10.1007/s00213-014-3704-1 Link zugegriffen am 07. August 2019
- Novel Drug Promising for Schizophrenia Nancy A. Melville April 03, 2015 Link zugegriffen am 07. August 2019
- NS Spectr. 2019 Feb;24(1):190-191. doi: 10.1017/S1092852919000245. 30 Lumateperone (ITI-007) for the Treatment of Schizophrenia: Overview of Placebo-Controlled Clinical Trials and an Open-label Safety Switching Study. Vanover K1, Glass S1, Kozauer S1, Saillard J1, Sanchez J1, Weingart M1, Mates S1, Satlin A1, Davis R1. Link zugegriffen am 07. August 2019
- Intra-Cellular Therapies Announces Positive Topline Phase II Clinical Results of ITI-007 for the Treatment of Schizophrenia Link zugegriffen am 07. August 2019
 Blog über Arzneimittel & Gesundheit Neues aus der Pharmawelt. Nachrichtne über neue Arzneimittel, Pharmazie und Gesundheit
Blog über Arzneimittel & Gesundheit Neues aus der Pharmawelt. Nachrichtne über neue Arzneimittel, Pharmazie und Gesundheit